Niniejszy przewodnik obejmuje zastosowania aseptycznych zbiorników na wodę ze stali nierdzewnej z operacjami krok po kroku do przechowywania PW/HPW, w tym zatwierdzone CIP/SIP, KPI i rozwiązywanie problemów.
Gotowy do specyfikacji lub aktualizacji? Przeglądaj modele zbiorników aseptycznychsparować z naszym System RO 1000 LPHi wybierz Membrany RO (4040/8040) np. ULP31-4040.
1) Streszczenie
- Kiedy wdrożyć: Używaj zbiornika aseptycznego, gdy PW/HPW musi utrzymywać pojemność buforową przy niskim ryzyku obciążenia biologicznego i zatwierdzonym czyszczeniu.
- Zwycięstwa operacyjne: zatwierdzone pokrycie CIP, integralność filtra odpowietrzającego, sterowanie "dead-leg", śledzenie trendów z alarmami i udokumentowane przełączanie.
- Szybka specyfikacja: 304/316L, RA≤0,8 µm (≤0,4 µm dla wyższego poziomu higieny), bezszczelinowe elementy wewnętrzne, urządzenie rozpylające dostosowane do pokrycia, hydrofobowy filtr odpowietrzający 0,2 µm z zaworem P/V.
2) Role systemowe i typowe przepływy
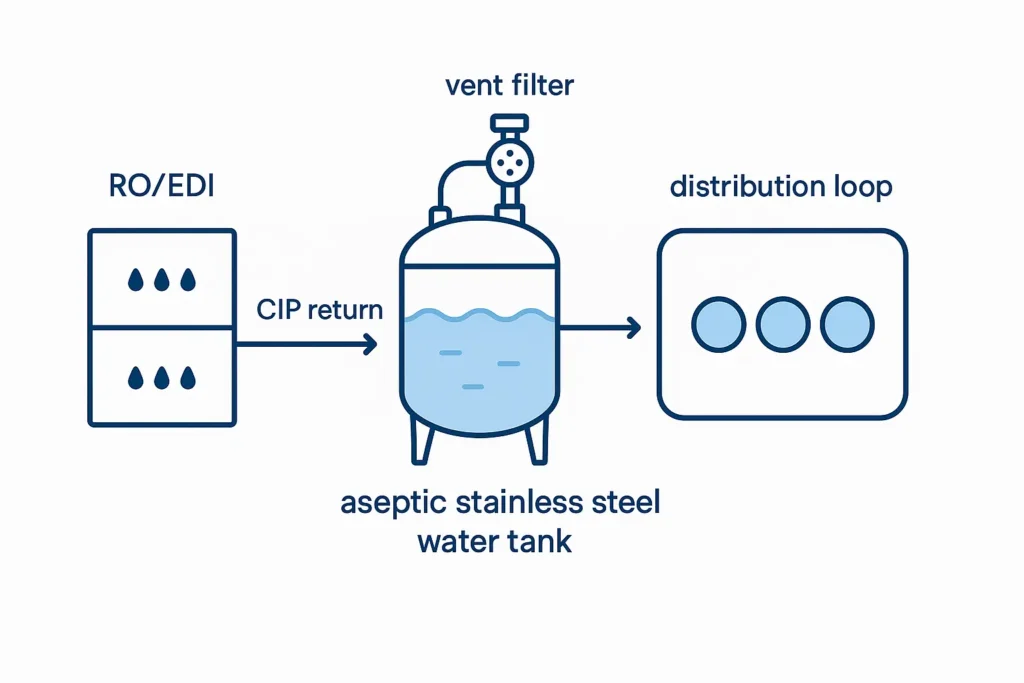
W większości roślin aseptyczny zbiornik na wodę ze stali nierdzewnej znajduje się pomiędzy RO/EDI a punktami użycia, zapewniając bufor, stabilizację ciśnienia i czasami mieszanie permeatu. Działa również jako węzeł powrotu CIP i odpowietrzania SIP. Pakiety upstream, takie jak nasz System RO 1000 LPH i wybór membran z piasta membranowa określenie jakości paszy, odzysku i chemii CIP.
3) Aplikacje według branży
3.1 Farmacja/biotechnologia (PW/HPW)
Zbiorniki zasilają pętle o temperaturze otoczenia lub kontrolowanej. Walidacja koncentruje się na wykończeniu powierzchni, pokryciu CIP, integralności filtra odpowietrzającego i trendach. Dobrze działający aseptyczny zbiornik na wodę ze stali nierdzewnej redukuje wzrost obciążenia biologicznego między RO/EDI a punktami użytkowania.
Lista kontrolna specyfikacji - 316L dla ryzyka chlorków; RA≤0,4 µm dla wysokiego poziomu sanitarnego; urządzenie rozpylające dostosowane do pokrycia ryboflawiną; filtr odpowietrzający 0,2 µm z portem integralności; nachylenie-dren; reprezentatywny zawór do pobierania próbek.
Wyzwalacze CIP - mikrobiologia trendów/konduktywność; wyniki ATP/swab; zaplanowane cykle według oceny ryzyka.
Najczęstsze pułapki - mokre filtry odpowietrzające, brak zimnych punktów podczas SIP, martwe nogi na trójnikach oprzyrządowania.
3.2 Napoje i nabiał
Składniki/mieszanka wody i uzupełnianie CIP zależą od przewidywalnej higieny zbiornika. Sezonowe wahania temperatury wody i obciążenie organiczne stanowią wyzwanie dla czyszczenia; płaszcz/izolacja i receptury stabilizują wyniki.
Lista kontrolna specyfikacji - 304 lub 316L według produktu; RA≤0,8 µm (≤0,4 µm w razie potrzeby); natrysk rotacyjny dla ciężkich zabrudzeń; izolowana powłoka; kontrola zapachu.
Wyzwalacze CIP - zmiana produktu, alerty sensoryczne/ATP, zaplanowane czynności sanitarne.
Najczęstsze pułapki - błony białkowo-tłuszczowe, przenoszenie smaków, niedogrzane cykle.
3.3 Kosmetyki i środki higieny osobistej
Lista kontrolna specyfikacji - kontrola zanieczyszczeń krzyżowych, kompatybilne uszczelki, zatwierdzone punkty końcowe płukania, identyfikowalność partii.
Wyzwalacze CIP - zmiany klasy formuły, filmy powierzchniowo czynne, pozostałości wizualne.
Najczęstsze pułapki - adsorpcja zapachów, skoki TOC po CIP, dryft urządzenia.
3.4 Czysta woda przemysłowa
Lista kontrolna specyfikacji - blokady pętli, alarmy przewodności, obejście dla konserwacji, redundancja dla krytycznych narzędzi.
Wyzwalacze CIP - trend przewodności/TOC, zaplanowane wyłączenia, wskaźniki biofilmu.
Najczęstsze pułapki - stagnacja podczas przestojów, błędy odpowietrzania, spadek podciśnienia podczas schładzania.
4) Codzienne operacje: SOP i listy kontrolne
4.1 Uruchamianie i przełączanie
- Kontrole przed użyciem: filtr odpowietrzający ∆P, stan urządzenia natryskowego, pozycje zaworów, linia bazowa przewodności.
- Opcje spłukiwania/odkażania zgodnie z URS; dokumentowanie przyczyn zmian (kodowanie przyczyny).
- Zapis: data, partia/linia, stan czyszczenia, alarmy od ostatniego uruchomienia.
4.2 Zadania zmianowe / dzienne / tygodniowe / miesięczne
| Cadence | Zadanie | Właściciel | Rekord |
|---|---|---|---|
| Zmiana | Wizualizacja, przewodność i kontrola temperatury; pozycja zaworu | Operacje | Arkusz dziennika |
| Codziennie | Wizjer urządzenia natryskowego; filtr odpowietrzający ∆P; pobieranie próbek (jeśli wymagane) | Operacje/QA | LIMS / dziennik |
| Co tydzień | Kontrola uszczelek; przegląd alarmów; wykresy trendów | Operacje | Bilet CMMS |
| Miesięcznie | Audyt wydajności CIP; weryfikacja przyrządów | QA/Eng | Formularz audytu |
4.3 Planowany a oparty na stanie CIP/SIP
Uruchamiaj zaplanowane cykle, ale zezwalaj na zastąpienia oparte na warunkach - punkty końcowe przewodności, wyniki ATP/swab i skoki trendów. Dokumentowanie receptur i kryteriów akceptacji; kontrola wersji receptur.
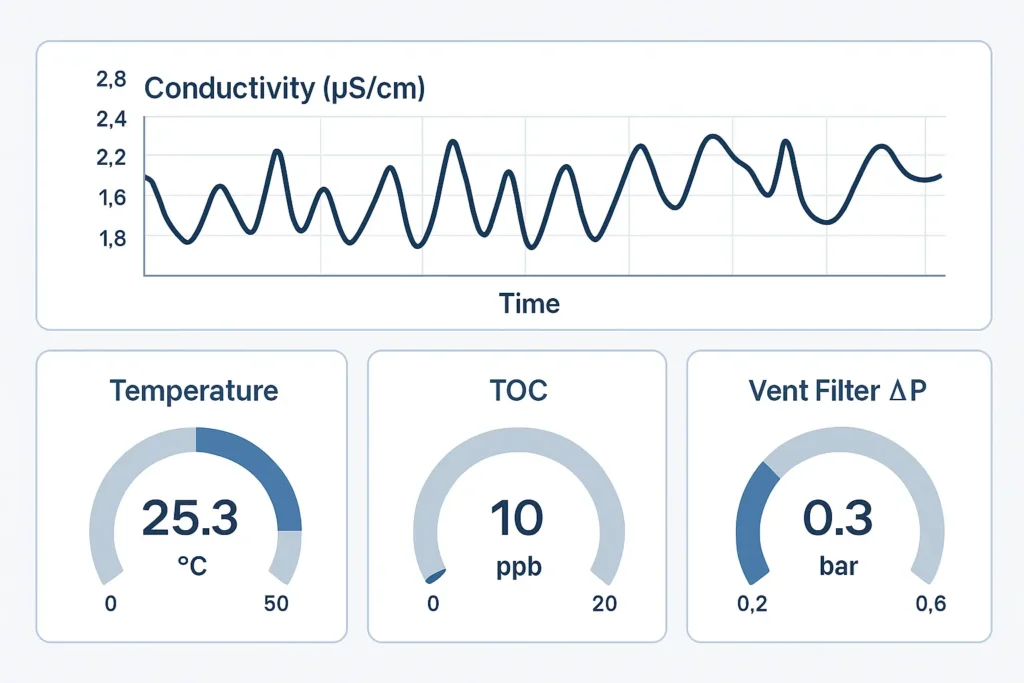
5) Monitorowanie i alarmy (wskaźniki KPI, które utrzymują zbiorniki w czystości)
- Przewodność (zasilanie, zbiornik, powrót pętli) - punkty końcowe płukania i stabilność.
- Temperatura - energia czyszczenia i wstrzymanie SIP.
- TOC (jeśli określono) - obserwacja pozostałości organicznych.
- Mikro trend - przekroczenia limitów działania.
- Filtr odpowietrzający ∆P - wskaźnik zwilżenia/zablokowania.
- Profile CIP - krzywe przepływu/ciśnienia/temperatury.

6) CIP/SIP w rutynowych operacjach (możliwe do podjęcia działania)
6.1 Wartości bazowe programu CIP
- Sekwencja: płukanie wstępne → zasadowe (40-70 °C) → płukanie → kwasowe (40-60 °C) → płukanie końcowe → opcjonalna pasywacja.
- Pokrycie: dobrać rozmiar pompy i urządzenia natryskowego zgodnie ze specyfikacją; zweryfikować z ryboflawiną w FAT i ponownie zweryfikować przy kontroli zmian.
- Punkty końcowe: przewodność liniowa dla płukania; w razie potrzeby dodać TOC.
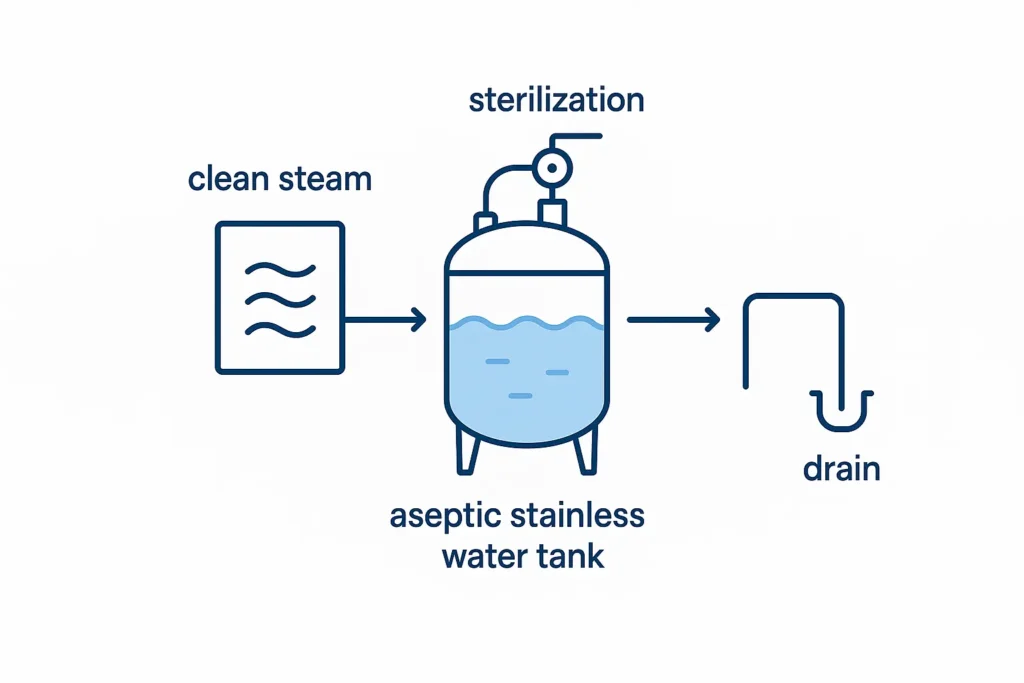
6.2 Najważniejsze elementy protokołu SIP
- Typowy reżim ~121 °C utrzymywany przez 20-30 min, mierzony w zimnym punkcie.
- Odpowietrzanie przez sterylny filtr; spuszczanie kondensatu; kontrola schładzania w celu uniknięcia spadku podciśnienia.
- Post-SIP: test integralności filtra odpowietrzającego (punkt pęcherzykowy) z zapisami.
Powiązane: System RO 1000 LPH - Pakiety uzdatniania wody - Membrany RO 4040/8040
7) Rozwiązywanie problemów i FMEA (szybkie drzewa)
7.1 Wzrost biofilmu
Objawy: dryft mikro/TOC; Przyczyny: Martwe nogi, niewystarczająca energia, długa bezczynność; Poprawka: gorętsze/dłuższe receptury, usuwanie martwych nóg, sprawdzanie prędkości pętli.
7.2 Zwilżanie / zapadanie się filtra odpowietrzającego
Objawy: wzrost ∆P, zdarzenia próżniowe; Przyczyny: zwilżanie kondensatem, nieprawidłowe ustawienie P/V; Poprawka: śledzenie ciepła lub podgrzewanie wstępne, właściwa krzywa chłodzenia, test integralności SOP.
7.3 Czerwień/korozja
Sprawdzić zgodność chemiczną, w razie potrzeby ponownie pasywować lub elektropolerować; zweryfikować limity chlorków i temperatury.
7.4 Dryft urządzenia
Zaplanuj kalibrację; dodaj dwukanałowe porównanie przewodności i temperatury.
8) Koszty i wydajność (bez narażania higieny)
- Odzyskiwanie i ponowne wykorzystanie roztworu CIP z zachowaniem limitów jakości.
- Stężenie równowagi w zależności od temperatury dla typu gleby.
- Łączenie partii/linii w celu skrócenia cykli start-stop.
- Śledzenie zużycia wody/energii/chemikaliów według CIP i benchmarkingu.
| Cykl CIP | Woda | Energia | Substancje chemiczne | Uwagi |
|---|---|---|---|---|
| Linia bazowa | 1.0× | 1.0× | 1.0× | Odniesienie |
| Odzyskane popłuczyny | 0.75× | 0.95× | 1.0× | Ponowne użycie płukania końcowego jako płukania wstępnego |
| Zoptymalizowana temperatura | 1.0× | 0.85× | 1.05× | Cieplejsze/krótsze tam, gdzie jest to dozwolone |
9) Dokumentacja i zgodność z przepisami (przede wszystkim operacje)
- Dzienniki pracy, zapisy partii CIP/SIP, raporty integralności filtrów odpowietrzających, kontrola zmian, matryca szkoleniowa.
- Pakiet QA: Certyfikaty EN 10204 3.1, mapa spoin, WPS/PQR, chropowatość powierzchni, próba hydrostatyczna, FAT/SAT.
Przydatne referencje branżowe: 3-A Normy sanitarne, Higieniczna konstrukcja EHEDG, Przegląd ASME BPE.
10) 30-60-90-dniowy plan adopcyjny
- 30d: SOP na żywo, pulpit nawigacyjny KPI, audyt CIP.
- 60d: Poprawki FMEA i działania związane z przyczynami źródłowymi; linia bazowa kosztów.
- 90d: ponowna walidacja i optymalizacja kadencji CIP; odświeżenie umiejętności.
11) Migawki przypadków
- Pharma PW 10 m³: 316L, RA≤0,4 µm, zwalidowany CIP, integralność filtra odpowietrzającego po SIP; wyeliminowane odchylenia.
- Mieszanka mleczna 30 m³: natrysk rotacyjny + płaszcz; osiągnięto stabilność sezonową; cotygodniowa sanityzacja zamiast codziennej.
- Elektronika PW 5 m³: blokady narzędzi; alarmy przewodności; skrócenie czasu przestojów podczas konserwacji.
12) Pliki do pobrania i RFQ
Zamów pakiet specyfikacji (GA + P&ID + lista materiałów) dostosowany do Twoich potrzeb w zakresie przepływu, wykończenia i CIP/SIP.
13) Najczęściej zadawane pytania
Jak często należy czyścić aseptyczny zbiornik na wodę w przemyśle farmaceutycznym?
Postępuj zgodnie z harmonogramami opartymi na ryzyku - często co tydzień lub co miesiąc - oraz z wyzwalaczami opartymi na trendach mikro/ATP i przewodności.
Co powoduje SIP a sanityzacja chemiczna?
Wybierz SIP, gdy wymaga tego śmiertelność termiczna lub walidacja; użyj odkażania chemicznego do procedur tymczasowych lub zakładów wrażliwych na temperaturę.
Jak zapobiec zwilżaniu filtra wentylacyjnego?
Podgrzać lub prześledzić ścieżkę odpowietrzania, spuścić kondensat, kontrolować chłodzenie i potwierdzić ustawienia zaworu P/V; przeprowadzić testy integralności po SIP.
Jakie wskaźniki KPI powinienem codziennie analizować?
Przewodność (zbiornik/pętla), temperatura, ∆P filtra odpowietrzającego, mikrotrend; dodać TOC, jeśli określono.
Czy mogę zmodernizować porty CIP/SIP i nadal przejść walidację?
Tak - kontrola zmian, ponowna weryfikacja pokrycia sprayem (np. ryboflawiną), aktualizacja receptur i kryteriów akceptacji oraz dokumentowanie wyników.

